

 |
 |
|
Навигация
|
Главная » Мануалы раммы, где оксиды стабильны, возможно растворение некоторого количества оксидов. Рапп [13, 20-22] й Стерн [23] определили кривые растворимости многих оксидов в NajSO в зависимости от давления SO3. Некоторые типичные кривые показаны на рис. 12.12. Следует заметить, что они, как правило, представляют собой кривые с минимумом, разделяющим области повышенной растворимости.
Рис.12.12. Результаты измерения растворимости оксидов с в расплаве NaSO при 927 °С и 1 атм (молярное содержание металлических ионов на 10* моль Na,SO.) [22] 5 7 9 П 13 isigaz Механизм развития горячей коррозии зависит, в первую очередь, от особенностей химического взаимодействия между расплавом осажденной соли и данным сплавом. В частности, именно присутствие соли является причиной появления на поверхности сплава продуктов такого взаимодействия, не обладающих защитными свойствами. Химические реакции могут быть вызваны изменением растворимости одних фаз в областях стабильности оксидов или образованием других фаз вне этих областей. При обсуждении возможных механизмов развития горячей коррозии удобно разделить их на две группы. В первую можно включить все механизмы, имеющие ту общую особенность, что образование продуктов химических реакций, не обладающих защитными свойствами, происходит в них вследствие некоторого флюсования сплава расплавом соли. Другая группа механизмов отличается тем, что в процессах образования продуктов химических реакций, не обладающих защитными свойствами, главную роль играют некоторые компоненты, входящие в состав осажденной соли (например, S или С1). Иногда влияние осажденного слоя на реакции в системе сплав-газ может быть и незначительным. В таких случаях осадок на поверхности сплавов часто формируется в виде пористой твердой фазы. Механизм развития 68 горячей коррозии при этом определяется типом реакций между сплавом и газовой фазой. Реакции флжования! солью Процессы, приводящие к потере барьерными слоями из продуктов химических реакций своих защитных свойств вследствие образования частиц, растворимых в жидкой осажденной соли, получили название реакций флюсования. Таких процессов может быть множество, но из всех возможных причин разрушения защитных барьерных слоев на поверхности сплавов следует особо отметить один важный механизм, который зависит от экспериментальных условий, таких как состав сплава и газовой фазы, температура и характеристики осадка. О кислотности или основности расплава сульфатного осадка можно судить по следующей реакции: (12.5) 80Г=80зН-02- с условием равновесия = S03V- (12.6) Уравнение (12.6) позволяет установить соотношение между давлением SO3 и активностью оксидных ионов на рис. 12.9 и 12.10. Величина К определяется стандартными свободными энергиями образования N82804, SO3 и NajO. Здесь - активность оксидных ионов в расплаве, равная активности NajO в этих расплавах. Аналогичные выражения можно написать и для расплавов других солей, таких, например, как карбонаты, гидрооксиды, нитраты и т.д. Кислотность сульфатов определяется давлением SO3 и увеличивается с его повышением. Нужная кислотность расплава достигается как изменением давления SO, в газовой фазе, так и другими способами, например, введением в систему примесей, влияющих на кислотность. Примером может служить ванадий, входящий как легирующий элемент в состав сплава или как загрязняющая примесь - в состав топлива. Оксид ванадия вступает в реакцию с N82804: Na,SO>V,0 ►2NaV03H-S03, (12.7) приводящую к изменению кислотности расплава. В сплавах, содержащих молибден и вольфрам, при окислении этих элементов в результате коррозии происходят аналогичные явления. Основное флюсование. Исходная концепция основного флюсования была предложена Бомщтейном и ДеКрессенте [24-26]. Позднее Гебель и Петтит [9] провели термодинамическое описание такой реакции применительно к случаю горячей коррозии никеля. Важной особенностью процесса является то, что удаление кислорода и серы из осажденной соли NaSO при ее химическом взаимодействии со сплавом приводит к образованию в ней оксидных ионов (см. рис. 12.9 и 1211). Они могут вступать в реакцию с оксидами металлов (МеО), которые в обычных условиях образуют на поверхности сплавов защитную пленку окалины МеО+О^ ►МеС^-, (12.8) и приводить к нарушению их защитных свойств. В зависимости от условий, существующих в расплаве, возможно повторное выпадение выделений оксидов. Процесс основного флюсования характеризуется целым рядом специфических особенностей. Так, процесс удаления серы из NaSO, необходимый для образования оксидных ионов, обычно сопровождается осаждением на поверхности сплава сульфидов. Кроме того, степень разъедания материала зависит от концентрации оксидных ионов в расплаве и, следовательно, для обеспечения непрерывности процесса разъедания требуется постоянная подпитка осажденного слоя свежими порциями расплава NajSO. Другими словами, процесс горячей коррозии с основным флюсованием во многих случаях является несамоподдерживающимся (см. рис. 12.8). И, наконец, он встречается, как правило, лишь в области высоких температур (выше 900 °С), так как при низких температурах процессы образования оксидных ионов протекают очень медленно. Вполне возможно также, что такая коррозия играет важную роль лишь в бескислотных газовых средах, не содержащих компонент типа SOj, хотя, если верна концепция Раппа я Гото [27], основное флюсование может происходить и в таких газах. Рапп и Гото [27] предположили, что оксидная окалина на поверхности сплава теряет свои защитные свойства лишь в 70 случае когда по сечению расплава осадка существуют отрицательные градиенты растворимости оксидов, так как только в таких условиях возможно непрерывное растворение и одновременное выпадение оксидов из расплава. Такой процесс протекает, например, при горячей коррозии никеля при 1000 °С на воздухе. Растворимость оксида никеля NiO по сечению слоя расплава соли меняется таким образом, что на границе раздела оксида с солью происходит его растворение в виде NiOf , а на границе соли с газом - выпадение в виде пористого NiO. Механизм Раппа-Гото, подходящий как для основного, так и кислого флюсования, не требует, чтобы источники или стоки для оксидных ионов обладали какими-либо особыми свойствами. Это весьма важное условие означает, что коррозионное разъедание может происходить и без постоянной дополнительной подпитки слоя осажденной соли. Шорес [28] провел справедливость критерия Раппа-Гото в разных условиях и показал, что самоподдерживающаяся реакция флюсования возможна далеко не во всех случаях. Например, при горячей коррозии никеля под слоем NaSO на воздухе при .1000 С расплав осадка на границе раздела с газовой фазой постепенно становится все более основным и, в конце концов, разъедание прекращается [9] и не возобновляется до тех пор, пока не будет осаждено дополнительное количество NaSO. Следует, однако, заметить, что для коррозионно-стойких сплавов более желательно, чтобы процесс горячей коррозии в них не был самоподдерживающимся, что позволяет избегать слишком сильной коррозионной деградации таких материалов. В условиях реальной работы деградация любых металлических систем происходит и без расплавленного осадка. Периодическое же осаждение в модифицирующий слой свежих порций соли, стимулирующее коррозионное разъедание материала в случае, когда процесс не является самоподдерживающимся, даже при очень малых скоростях осаждения будет ускорять формирование на поверхности сплава нестойких слоев из продуктов химического взаимодействия осадка со сплавом взамен защитных барьерных слоев. Кислое флюсование. Кислое флюсование [29, ЗО] представляет собой процесс формирования на поверхности сплава оксидного слоя окалины, не обладающего защитными свойствами, который протекает вследствие передачи оксидных ионов из оксидов, образующихся на поверхности этого сплава без осадка, в расплав осажденной соли: МеО ►Ме2++0-. (12.9) Расплав может становиться кислым, как минимум, по двум причинам. Во-первых, из-за присутствия в газовой фазе компонентов, повышающих кислотность расплава. И, во-вторых, из-за Наличия в самом сплаве оксидов составляющих его элементов. В зависимости от этого различают газофазное или-твердофазное кислое флюсование соответственно. Газофазное кислое флюсование. При газофазном кислом флюсовании компонента, вызывающая повышение кислотности расплава, попадает в жидкий осадок из газа. Примером могут служить пары SO3 и VjOj. Как только они попадают в жидкий осадок, начинают идти реакции: 80з+80Г=820Г; (12.10) VA + SOr = 2VO; + SO3. (12.11) Газофазное кислое флюсование имеет некоторые характерные особенности. Во-первых, чаще всего оно наблюдается, по крайней мере, при стимулированном SO3 разъедании, в температурном интервале 650-800 °С, из-за чего получило название низкотемпературного или горячей коррозии П рода. Такие невысокие температуры нужны для образования сульфатов типа CoSO, NiSO и Alj(S04)3 (не обязательно с единичной активностью), которое при более высоких температурах требует повышения давления SO3, в то время, как во многих газовых средах, образующихся при сжигании топлива, повышение температуры часто приводит к падению давления SO3. Во-вторых, горячая коррозия, связанная с газофазным взаимодействием, сопровождается вполне определенными изменениями микроструктуры материала, которые зависят от состава сплава и агрессивной среды. Типичные примеры деградации структуры CoCrAlY сплава представлены на микрофотографиях на рис. 12.1, г и 12.13. Из фотографий видно, что перед коррозионным фронтом практически нет областей обедненного сплава (рис. 12.13), а сера если и обнаруживается среди продуктов коррозии, то лишь вблизи границы раздела между сплавом и продуктом коррозии и всегда в связанном с кислородом виде. При добавлении в 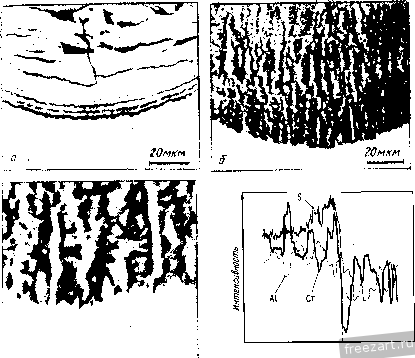 продут коррозии CnmS подложки г Рис.12.13. Микроструктурные особенности сплава CoCrAlY, возникшие в процессе 15,3-4 выдержки при 704 ос и осадке Na2S04 2,5 мг/см в атмосфере кислорода с примесью (7Х10-< атм) SO3: о - следы перемещения коррозионного фронта; б, е - вид а Со-фазы в сплаве; г - результаты микрорентгеноспектрального анализа продуктов коррозии состав сплав никеля сера легко обнаруживается на микрофотографиях стурктуры в виде отдельных сульфидных фаз. Для объяснения стимулированной газофазным взаимодействием горячей коррозии были предложены три модели. В первой из них [31-34] образование на поверхности сплава не обладающих защитным действием окалин типа AljOj и CTjO, объясняется быстрым удалением кобальта и никеля из поверхностных слоев сплава в осажденный расплав соли. Это приводит к нарушению сплошности растущих оксидных AI2O3 и СГ2О3 пленок. Обеднение же сплава кобальтом и никелем происходит из-за растворения их оксидов в кислом расплаве, хотя у поверхности осадка эти оксиды сохраняют свою стабильность. В другой модели [35] предполагается, что давление кислорода над поверхностью сплава под слоем осадка слишком мало для образования оксидов кобальта или никеля. Более того, это давление мало настолько, что происходит образование значительной концентрации ионов SO : SOr=SC-+l/202. (12.12) Считается, что оксид алюминия AlOj нестабилен в таких расплавах, так как на границе раздела сплав-расплав пре-имушественно протекает реакция: 3SO3+AI2O3- -2AP++3S0-. (12.13) Образование не обеспечивающих защиту частиц оксидов происходит в удаленных от поверхности сплава областях расплава, где давление кислорода выше. Эта модель, однако, уязвима, так как совсем не очевидно, что при низком давлении SO которое требуется для предотвращения образования оксидов кобальта и никеля, осадок будет жидким. С другой стороны, анализ микроструктуры после коррозии показывает, что в областях сплава на границе раздела с продуктами коррозии оксидов кобальта и никеля нет (рис. 12.13, в). Третья модель [36-38] предполагает образование на границе между сплавом и продуктами коррозии сульфидов, в результате окисления которых формируются незащищающие оксидные фазы. Типичный пример такой структуры показан на рис. 12.4. Нет никаких сомнений, что в сплавах с высоким содержанием никеля реализуется именно этот механизм. В то же время он невозможен в сплавах кобаль-хром-алюминий. Важно определить применимость всех этих моделей в зависимости от состава сплавов и условий проведения низкотемпературных испытаний на горячую коррозию. Твердофазное кислое флюсование. При твердофазном кислом флюсовании повьццение кислотности расплава вызывается попаданием в него оксидов таких элементов как молибден [29, 39], вольфрам [ЗО] или ванадий [ЗО]. Типичными реакциями при этом будут: М0+З/2О2 --МоОз, МоОз+SC-- >MoOf+SO3, AIJO3+3M0O3-►2AF++3M0O2-, (12.14) (12.15) (12.16) где AI2O3 растворяется в областях расплава с высокой активностью М0О3 и выделяется там, где она мала, например, вблизи поверхности расплава, откуда М0О3 уходит в газовую фазу. При кислом флюсовании сам осадок может стать кислым, как, например, в случае осадка NajSO с повышенным содержанием NajMoO; NajSO может полностью перейти в NajMoO с увеличением количества М0О3 в NajMoO [39]. При твердофазном кислом флюсовании обычные защитные оксиды могут уничтожаться путем их необратимого или обратимого, с последующим выпадением в осадок уже в виде незащищающих оксидов, растворения в расплаве. Мисра [40] исследовал коррозию никелевых суперсплавов с молибденом под слоем NajSO при 950 °С и пришел к выводу, что твердофазное кислое флюсование в этом случае протекает по механизму, близкому к предложенному Лутра [31-34], согласно которому в кислом расплаве происходит образование ионов Ni* и выделение NiO на границе раздела расплава с газом. Формирование сплошных пленок AI2O3 и СГ2О3 на поверхности сплава в этом случае невозможно из-за обеднения сплава никелем. Как и для многих других процессов развития коррозии в настоящее время еще невозможно сделать окончательное заключение о механизме твердофазного флюсовании. Наиболее существенной особенностью твердофазного кислого флюсования является его самоподдерживающийся характер, что делает возможным полное разрушение сплава даже после однократного осаждения жидкого осадка. Такой эффект часто наблюдается в конструкционных сплавах, упрочнение твердого раствора в которых вызывается элементами, оксиды которых могут повышать кислотность расплава. Твердофазное кислое флюсование обычно происходит при высоких температурах, что связано с необходимостью интенсивного окисления тугоплавких металлов для получения сколь-нибудь значительного количества оксидов, повышающих кислотность расплава. Нередко до начала твердофазного кислого флюсования протекает другая стадия развития коррозии [41]. Именно на этой первой стадии расплав насыщается оксидами тугоплавких металлов. Горячая коррозия, стимулированная компонентами осадка Еще одной важной характеристикой процесса горячей коррозии является понижение активности кислорода над повер- хностью сплава под слоем осажденной на ней соли. Это происходит как вследствие наличия в составе сплава элементов, имеющих высокое сродство к кислороду, так и из-за затрудненности доступа кислорода к поверхности сплава, вызванной необходимостью его диффузии через слой осадка (см. рис. 12.9). В результате условия взаимодействия остальных элементов в осадке с элементами сплава становятся более благоприятными. Вообще говоря, на процесс горячей коррозии могут влиять очень многие элементы, входящие в состав осадка. Наиболее сильное влияние оказывают сера и хлор. Влияние серы. По причинам, рассмотренным ранее (см. рис. 12.4), в сплаве под слоем расплавленного осадка возможно образование значительного количества сульфидных фаз, особенно при повышенных температурах. По мере окисления сульфидов на их месте появляются фазы, не обладающие защитными свойствами. Это наблюдалось еще при первых исследованиях горячей коррозии материалов для газовых турбин [42, 43]. Такая горячая коррозия, происходящая в результате окисления сульфидов, получила название сульфи-дации. Важно отметить, что сульфидация происходит далеко не всегда. То, что механизм горячей коррозии при сульфи-дации связан с окислением сульфидов, не вызывает никаких сомнений (рис. 12.14). Из-за изменения давления SO при окислении происходит образование оксидов, не способных 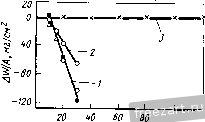 700 N Рис.12.14. Сплав Ni-25Сг-6А1. Сравнение результатов циклического окисления при 1000 °С (длительность цикла - 1ч) сплава с поверхностным осадком N82804 (i) и сплава, предварительно сульфурированного (о) в газовой смеси H2S-Hj. Осадок N82804 5 мг/см наносили первый раз после 5-ч выдержки, затем после 20 ч и затем через каждые 10 ч. Сульфурирование проводили по тому же расписанию, что и нанесение N82804; поглощение серы было при этом эквивалентно таковому в контакте с осадком N828O4 5 мг/см (5 - обычное циклическое окисление) 76 обеспечить защиту поверхности, а частицы этих оксидов находятся В растянутом состоянии [44]. Ранее при исследовании процесса горячей коррозии в качестве газообразного реагента часто использовали килород. При изучении низкотемпературной горячей коррозии II рода широко применялась газовая смесь Oj-i-SOj. Все эти исследования [37, 38] показали, что механизм сульфидации играет важную роль во всем температурном интервале существования горячей коррозии. При более низких температурах коррозионная деградация материала за счет сульфидации возможна лишь при наличии SOj в газовой фазе. Влияние хлора. Присутствие хлора в осадке может влиять на горячую коррозию сплавов двумя путями. Во-первых, при концентрациях хлора порядка 10 % (ат.) возрастает склонность существующих на поверхности сплавов оксидных окалин (например, AI2O3 и CrjO,) к растрескиванию и скалыванию [45]. Это вызывает быстрый переход к стадии развития коррозионной деградации сплава даже при кратковременном воздействии агрессивной среды. Во-вторых, установлено, что высокое содержание хлора в осадке вызывает быстрое обеднение сплава алюминием и хромом [10, 35]. Типичные результаты показаны на рис. 12.7, где легко видеть, что с повышением содержания хлора разъедание сплава усиливается. Наличие в осадке хлоридов вызывает развитие пористости или появление каналов в сплавах по мере их обеднения хромом и алюминием и образование на их поверхности совершенно незащищающих сплав оксидов этих элементов. Этот процесс во многом похож на процесс селективного выщелачивания цинка из медно-цинковых сплавов во время децинкования [46]. Бесспорно, что присутствие хлоридов в составе осадка приводит к усилению горячей коррозии материала. Сразу после обнаружения явления низкотемпературной горячей коррозии материалов газовых турбин очень многие исследователи были склонны приписать его влиянию хлоридов, присутствующих в осадке. И хотя это влияние действительно может быть весьма значительным, все-же многочисленные данные свидетельствуют, что низкотемпературная горячая коррозия возможна и без хлоридов. Ее появление скорее связано с относительно высоким давлением SO3 в газовой фазе и с образованием назащищающих оксидов на поверхности материала под действием кислого жидкого осадка. Следует, однако, отметить, что значительная часть данных по горячей коррозии II рода получена при стендовых испытаниях или лабораторных испытаниях в трубчатых печах, условия при которых заметно отличаются от реальных условий работы материалов в газовых турбинах [47]. Поэтому заранее влиянием хлоридов пренебрегать не следует. При появлении условий, благоприятствующих проявлению влияния хлоридов, коррозионное разъедание во всем интервале температур от низких, таких как 700 °С до примерно 1000 °С резко усиливается [48]. 12.5. Эффекты, связанные с влиянием на горячую коррозию различных химических элементов Прежде чеМ' обсуждать влияние на горячую коррозию различных химических элементов полезно будет обобщить все известные сведения о механизмах развития горячей коррозии с указанием условий, при которых они становятся доминирующими. На рис. 12.15 представлена схематическая диаграмма, показывающая основные механизмы горячей коррозии и их специфические особенности, а на рис. 12.16 - области температур и составы газовой среды, при которых они доминируют. Здесь важно подчеркнуть, что при высоких температурах длительность начальной стадии горячей коррозии больше, чем при низких, и это следует учитывать при сравнении скоростей горячей коррозии при разных температурах. Значения скоростей, приводимые для разных механизмов на рис. 12.16, измерены уже на стадии развития горячей коррозии. Как видно, коррозионное разъедание при низких температурах сильнее, когда в газовой фазе присутствует SO3. Это связано с тей, что если SO3 отсутствует, осадок часто не становится жидким; таким образом, присутствие SO3, способствующее формированию жидкофазного осадка, вызывает гораздо более сильное разъедание при пониженных температурах. Сульфидация возможна во всем температурном интервале, но как и в предыдущем примере, вызываемое ею разъедание при пониженных температурах не столь значительно, если осажденный слой конденсируется не как жидкая фаза. Температурные области доминирования других механизмов были выбраны на основании приведенных ранее в этой главе сведений. Эта схема не учитывает влияние хлорида натрия. 78 Осадок не реагирует с подлотной Защитная окалина нарушается В процессе обычного окисления Условия шлакования ((ртсоВания) В контакте с осадком Основная средо i---- Нарушение окалины из-за реакции, В которых участвуют оксидные ионы Кислая среда Наоишение окалины благодаря реакциям с участием SOj, V2O5, 0з ГазоВая (раза СплоВ SO3 V?05 поставляются к осадку с газовым потоком Mo03,W03,V205 поставляются к осадку 8 результате окисления сплова Компоненты осодка накапливаются всплоВе Другие компоненты Нарушение окалины В результате окиспения сульфидов Нарушение окалины в результате реакций с оксидани ипиииипчп ,----- Рис.12.15. Схематическое представление механизмов нарушения защитной окалины у сплавов, проявляющих благодаря избирательному образованию барьерных оксидных слоев повышенное сопротивление высокотемпературному окислению и горячей коррозии Рис.12.16. Схема, иллюстрирующая температурные диапазоны и составы газовой фазы, в пределах которых приобретают определяющее значение механизмы распространения горячей коррозии: 1 - кислое шлакование посредством реакш1й с газовой фазой: сульфурирование; 2 - кислое , шлакование посредством реакций со сплавом; основное шлакование; сульфурирование; 3 - смесь Oj-SO3 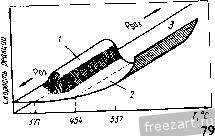 При высоких температурах вызываемое хлоридом разъедание эквивалентно действию других механизмов развития коррозии. При пониженных температурах он определенно будет вызывать более сильное разъедание, чем NaSO, если только в газовой фазе не будет SO,. Если же SO3 присутствует в газовой фазе, то NaCl будет превращаться в NajSO; однако на воздухе вызываемое NaCl разъедание Может быть столь же сильным, как и разъедание вызываемое NajSO в SO, при низких температурах. При горячей коррозии П рода формируется специфическая микроструктура (см. рис. 12.1, г и 12.13). Коррозионное разъедание при низкой температуре может происходить путем газофазного кислого флюсования, сульфидации или за счет влияния хлоридов. Обычно под характерной микроструктурой подразумевается структура, формирующаяся при коррозии в интервале 650-850 °С при наличии SO, в газовой фазе. При этих условиях развивается процесс газофазного кислого флюсования или сульфидации, в зависимости от состава сплава. Высокотемпературная горячая коррозия или коррозия I рода, происходит в интервале 800-1000 °С и вызывает формирование микроструктуры, показанной на рис. 12.1, б, 12.1, в или 12.4. Одна может протекать .за счет основного флюсования, сульфидации или твердофазного кислого флюсования. Ниже рассмотрено влияние различных химических элементов на горячую коррозию сплавов. Классификация проведена по механизмам развития коррозии, представленным на схеме на рис. 12.15. Как следует из вышеизложенного, доминирующий механизм развития коррозии в каждом конкретном случае определяется условиями испытания. Основное флюсование Как никель, так и кобальт чувствительны к коррозионному разъеданию путем основного флюсования. В их поведении нет сколь-нибудь значительной разницы [9, 49]. Горячая коррозия чистого железа не изучена, так как при температурах выше приблизительно 650 °С железо очень быстро окисляется даже в отсутствие условий для горячей коррозии. Эффекты, связанные с другими элементами, будут рассмотрены в той степени, в какой эти элементы влияют на сплавы на основе никеля, кобальта и железа. 80 Хром подавляет разъедание за счет основного флюсования в сплавах на основе никеля, кобальта и железа. Он вызывает понижение концентрации оксидных ионов до уровня, при котором взаимодействие с NiO, СоО и, возможно, оксидами железа становится невозможным. Если концентрация хрома достаточно высока для образования защитной окалины CtjOj, сопротивление сплава горячей коррозии заметно возрастает. Алюминий подавляет основное флюсование, если его концентрация достаточна высока для образования сплошной окалины AljOj. Однако, в отличие от хрома, он не предотвращает разъедания NiO и СоО окалин оксидными ионами. Титан не оказывает никакого заметного влияния на коррозионную деградацию сплавов на основе никеля, кобальта или железа, если она происходит по механизму основного флюсования. Однако исследования влияния этого элемента были немногочисленны. Тугоплавкие элементы, такие как молибден, вольфрам и ванадий, могут подавлять основное флюсование [50]. Оксиды этих элементов взаимодействуют с оксидными ионами и таким образом подавляют их взаимодействие с AljO NiO, СоО и т.д. Эффект сходен с влиянием хрома, но при использовании молибдена, вольфрама и ванадия для подавления основного флюсования существует опасность появления кислого флюсования. Тантал также способен подавлять основное флюсование, но менее эффективно, чем хром. В то же время в противоположность другим элементам, упрочняющим твердый раствор, таким как молибден, вольфрам и ванадий, он не вызывает кислого флюсования. Другие элементы, встречающиеся в составе суперсплавов или их покрытий, не оказывают явно выраженного влияния на горячую коррозию сплавов за счет основного флюсования. Покрытия, на которых в процессе работы образуется окалина из диоксида кремния, нежелательны из-за очень высокой чувствительности диоксида кремния к основному флюсованию. Газофазное кислое флюсование Практически все сплавы чувствительны к газофазному кислому флюсованию. Сплавы на основе кобальта немного более чувствительны, чем никелевые или железные сплавы из-за большей стабильности CoSO по сравнению с NiSO и FeSO, однако практического значения эта разница не имеет. . Окалина AljOj, сушествуюшая на поверхности сплава, подавляет процесс газофазного кислого флюсования, но лишь до тех пор, пока он не переходит в стадию развития и в этом случае скорость горячей коррозии уже мало зависит от концентрации алюминия в сплаве. В то же время исследования микроструктуры показали, что коррозионное разъедание в этом случае преимушественно распространяется по богатым алюминием фазам [36]. Увеличение концентрации хрома в сплаве не увеличивает длительность начальной стадии газофазной кислой коррозии, однако вызывает снижение скорости коррозии на стадии развития [51]. Из литературных данных можно сделать вывод, что кобальт-хромовые сплавы обладают прекрастной стойкостью против низкотемпературной горячей коррозии [34]. Некоторые кислородо-активные элементы (например, Y), добавляемые в сплавы для улучшения сцепления оксидной окалины с металлической подложкой, являются слабыми местами, по которым расплавленный осадок может проникать сквозь защитную пленку окалины [52]. Оксиды таких элементов часто как струны проходят через всю толщину окалины AI2O3 и легко вступают в реакцию с кислым расплавом осадка. В сплаве, однако, существуют и другие слабые места, через которые соль может проникать через оксидную пленку [52], так что само по себе присутствие в сплаве кислоро-до-активных элементов не слишком заметно сказывается на снижении длительности начальной стадии коррозии. Большинство других элементов, присутствующих в суперсплавах и материалах покрытий этих сплавов, не оказывают сколь-нибудь значительного влияния на процесс газофазного кислого флюсования. Исключительно высоким сопротивлением кислотному флюсованию обладает окалина диоксида кремния, формирующаяся на поверхности некоторых покрытий. Эти оксиды слабо растворимы в кислых расплавах (рис. 12.12) и такие защитные окалины часто образуются на сплавах с достаточно высоким содержанием кремния. Использованию таких окалин как части системы защиты сплавов препятствует, однако, их высокая чувствительность к коррозионной деградации за счет основного флюсования. 82 Твердофазное кислое флюсование Твердофазное кислое флюсование связано с присутствием в составе сплава некоторых тугоплавких элементов, особенно молибдена, вольфрама и ванадия. Для предотвращения такой формы горячей коррозии необходимо поддерживать концентрацию этих элементов на достаточно низком уровне. Точное значение допустимой концентрации зависит от условий работы сплава. Практически нет никакой разницы в коррозионном разъедании сплавов на основе никеля, кобальта и железа, имеющих в своем составе тугоплавкие элементы. За исключением хрома все другие элементы не оказывают никакого заметного влияния на процесс твердофазного кислого флюсования. Однако так как для стимулирования этой формы горячей коррозии требуется достаточно сильное окисление тугоплавких металлов, то все элементы, способствующие селективному окислению алюминия или хрома в составе суперсплава, в известном смысле могут рассматриваться как примеси, подавляющие твердофазное кислое флюсование. Горячая коррозия под действием серы (сульфидация) Горячая коррозия, обусловленная присутствием, серы, часто протекает в виде основного флюсования, так как за счет формирования сульфидов в сплавах в расплаве осадка происходит образование оксидных ионов. Как можно видеть на рис. 12.13, некоторые никелевые сплавы гораздо более чувствительны к такому виду горячей коррозии, чем кобальтовые сплавы. Отсюда можно сделать вывод, что сплавы на основе кобальта обладают более высоким сопротивлением горячей коррозии, чем сплавы никеля. Однако такое утверждение в общем неверно и справедливо лишь для некоторых видов горячей коррозии. Разница в коррозионном разъедании при высокотемпературных испытаниях сплавов на основе никеля и кобальта, содержащих хром и алюминий (см. рис. 12.3), еще ничего значит. Увеличение концентрации хрома или алюминия в этих сплавах приводит к увеличению времени до начала стадии быстрой сульфидации. Сплавы на основе никеля, однако, приобретают очень высокую восприимчивость к коррозионному разъеданию при уменьшении концентрации алюминия в них <6 % (по массе). В таких сплавах происходит быстрое удаление серы из осажденного слоя, сопровождающееся очень сильным разъеданием сплава за счет образования сульфидных фаз (рис. 12.17). Все остальные элементы, кроме хрома и алюминия, входящие в состав суперсплавов, не оказывают существенного влияния на стимулированную серой горячую коррозию. Имеются данные, свидетельствующие о важном значении отнощения концентраций титана и алюминия [53], однако роль титана остается неясной и, возможно, все результаты следует отнести лищь на счет влияния алюминия. 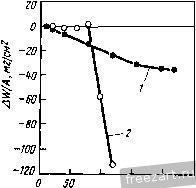 Рис.12.17. Временная зависимость изменений LWlA при циклической горячей коррозии сплавов Ni-ЗОСг (7) и Ni-30Cr-6Al (2) с осадком NajSO 5 мг/см (продолжительность циклов - 1ч) при 1000 °С и 1 атм Oj. Al сначала придает сплаву Ni-ЗОСг-6А1 более высокую стойкость, чем у Ni-ЗОСг, однако при более длительном oкиcлeiIии способствует более интенсивному коррозионному воздействию т т 200 N Другие механизмы развития горячей коррозии В табл. 12.1 обобщены данные по влиянию основных элементов, входящих в состав суперсплавов, на различные механизмы развития горячей коррозии. В случае механизма, связанного с хлоридами в осадке, единственными элементами, оказывающими благоприятное влияние, являются титан и платина [54]. Кроме отмеченных, возможно и другие механизмы развития горячей коррозии. Так, например, некоторые исследователи полагают, что существенный вклад в процесс деградации при горячей коррозии деталей газовых турбин могут вносить частички углерода, соударяющиеся с поверхностью материала [55]. 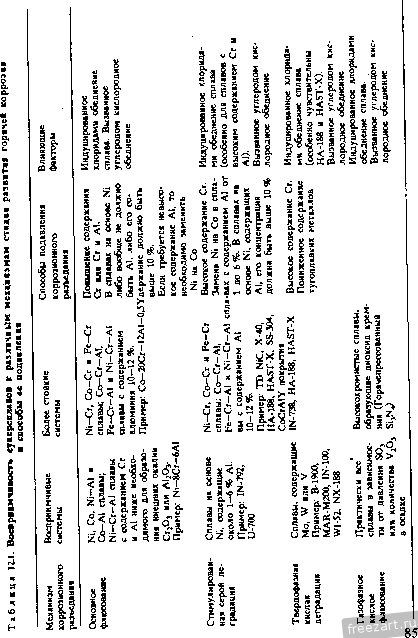 12.6. Стойкость к разъеданию при горячей коррозии некоторых суперсплавов Полезно провести сравнение стойкости разных суперсплавов к горячей коррозии. Коррозионное разъедание суперсплавов зависит от их состава и других факторов, определяющих условия проведения испытания или работы. Оценить стойкость суперсплавов к коррозионному разъеданию можно путем сравнения их работоспособности при фиксированных условиях работы. При этом, однако, возникают сложности, связанные с различной длительностью начальной стадии горячей коррозии в разных сплавах. Эта стадия определяет время, необходимое для начала стадии развития горячей коррозии. Например, считается, что сплав IN-738 обладает более высокой стойкостью к горячей коррозии, чем В-1900. Анализ данных показывает, что это скорее связано не с более низкой, чем у В-1900, скоростью горячей коррозии на стадии развития, а с более продолжительным временем инициации этой стадии в IN-738. Разумно предположить, что как только горячая коррозия суперсплавов переходит в стадию развития, скорость разъедания материала становится с практической точки зрения недопустимо большой при любых механизмах развития коррозии. Следовательно, основной параметр, по которому имеет смысл проводить сравнение стойкости суперсплавов к горячей коррозии и который определяет эту стойкость, это время, необходимое для инициации стадии развития коррозионного разъедания, то есть длительность начальной стадии горячей коррозии. К сожалению, во многих литературных источниках среди данных по горячей коррозии суперсплавов время до начала инициации коррозионного разъедания не приводится. С другой стороны, изготовители газовых турбин вполне понимают ва.жность этого фактора и при выборе сплавов для узлов и деталей турбин пользуются собственными источниками информации. Перед тем, как перейти к сравнению стойкости к горячей коррозии разных суперсплавов, важно подчеркнуть, что в этих сплавах очень часто после инициации коррозионного разъедания процесс может развиваться в несколько стадий. Такое поведение было отмечено для сплавов В-1900 [29] и IN-738 [41]. В сплаве В-1900 стадия развития протекает за счет основного флюсования с последующим переходом к меха-86 низму твердофазного кислого флюсования. Аналогичные результаты были получены и на других сплавах с таким же, как и в В-1900, содержанием хрома, алюминия и молибдена. Протекание стадии развития горячей коррозии в несколько этапов возможно характерно для больщинства суперсплавов. Если проводить сравнение стойкости суперсплавов к горячей коррозии по времени перехода разъедания к стадии развития, то определение этапов протекания этого процесса не обязательно. Наиболее важным элементом, обеспечивающим стойкость суперсплавов к горячей коррозии, является хром (табл. 12.1). Этот элемент подавляет коррозионное разъедание независимо от действующего механизма горячей коррозии, хотя в случае стимулированной хло^)идами коррозии его эффективность и не так высока. Следующей по важности переменной, связаннной с химическим составом суперсплавов, является концентрация тугоплавких металлов, которую следует поддерживать на минимально необходимом уровне. Однако, если концетрация хрома в сплаве повышена, то и содержание тугоплавких элементов может быть увеличено (например, сплавы Hastelloy X, Haynes 188). Тантал не оказывает такого вредного влияния на стойкость сплавов к горячей коррозии, как молибден, вольфрам и ванадий. Третий важный фактор при разработке коррозионно-стойких сплавов - это содержание в них алюминия. В материалах покрытиий концентрация алюминия может достигать 10% и более, и при этом возможно достижение благоприятных эффектов. В конструкционных суперсплавах, однако, концентрация алюминия не может превышать 6 %. При содержании алюминия от 2 до 4 % суперсплавы на основе никеля становятся слишком чувствительны к такому виду коррозионной деградации, как сульфидация. Не обнаружено никакой заметной разницы в стойкости суперсплавов к низкотемпературной горячей коррозии. Несколько лучшие свойства показывают сплавы с высоким содержанием хрома (например, ~20 %), но разница невелика. По отношению к высокотемпературной горячей коррозии более стойкими являются суперсплавы с высоким содержанием хрома и пониженным содержанием тугоплавких металлов. Кроме того, в сплавах на основе никеля концентрация алюминия не должна быть слишком большой при невысоких концентрациях 1 2 3 4 5 6 7 ... 19 |
 |
 |